電子常磁性共鳴 (EPR) の基本概念
電子常磁性共鳴 (EPR) は、不対電子の磁気モーメントから生まれた磁気共鳴技術です。原子や分子に含まれる不対電子を定性的および定量的に検出し、周囲の環境の構造特性を調べるために使用できます。フリーラジカルの場合、軌道磁気モーメントの影響はほとんどなく、総磁気モーメントの大部分 (99% 以上) は電子スピンによって寄与されるため、電子常磁性共鳴は「電子スピン共鳴」(ESR) とも呼ばれます。
その物理的原理は核磁気共鳴に似ていますが、EPR は陽子などの他の核スピンではなく、不対電子に焦点を当てています。EPR は主に、フリーラジカル、格子欠陥、遷移金属および希土類金属イオン、三重項分子の検出に使用されます。また、物質の原子や分子に含まれる不対電子を定性的および定量的に検出し、周囲の環境の構造特性を調べるためにも使用できます。
電子常磁性共鳴(EPR)の基本原理
電子は一定の質量と負電荷を持つ基本粒子で、2種類の運動を行うことができます。1つは原子核の軌道の周りを移動すること、もう1つは原子核の中心軸を回転することです。
電子の移動によりトルクが発生し、移動中に電流と磁気モーメントが発生します。外部の一定磁場Hでは、電子の磁気モーメントの効果は小さな磁気棒または磁気針のようなものです。電子のスピン量子数は1/2であるため、電子は外部磁場内で2つの方向しかありません。1つはHに平行で、低エネルギーレベルに対応し、エネルギーは-1/2gβHです。もう1つはHの逆数に平行で、高エネルギーレベルに対応し、エネルギーは+1/2gβHで、2つのレベル間のエネルギー差はgβHであり、図1に示すようにゼーマン効果と呼ばれます。
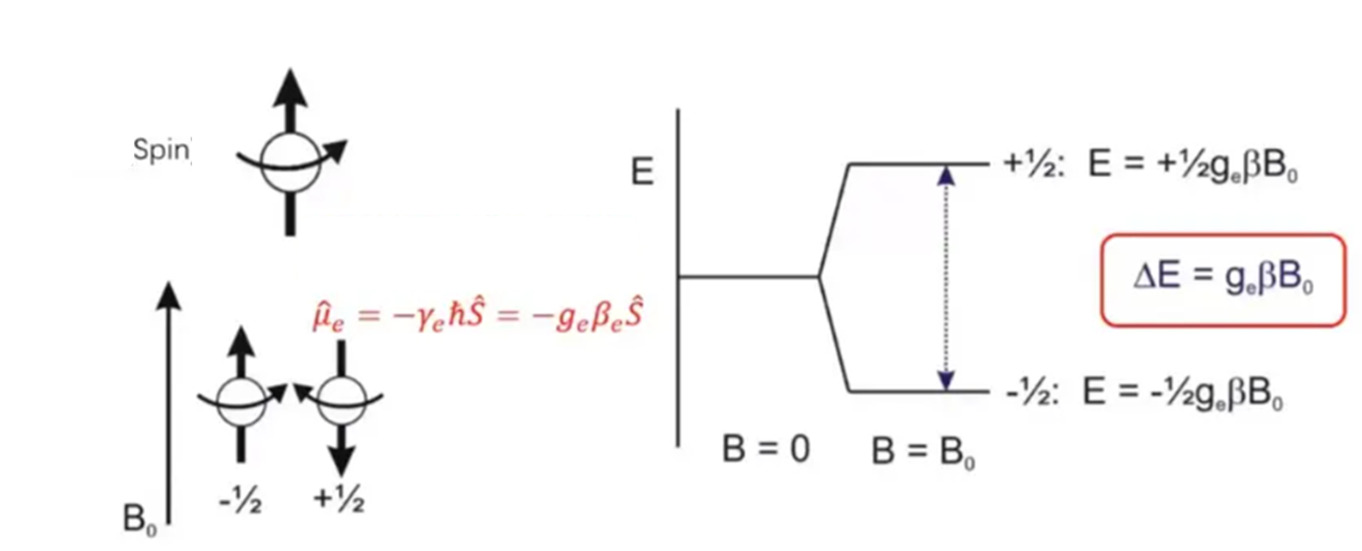
図 1 静磁場中の電子のゼーマン効果
周波数 v の電磁波を H に垂直な方向に印加し、条件 hv=gβH(B) を満たすと、図 2 に示すように、低レベルの電子が電磁波エネルギーを吸収して高レベルに遷移します。これを電子常磁性共鳴と呼びます。
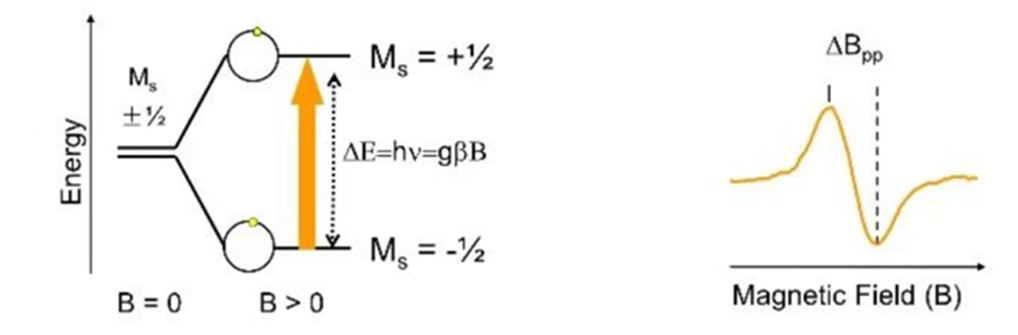
図2 共鳴吸収図
電子常磁性共鳴の発生に関する上記の基本条件において、h はプランク定数、g はスペクトル分割係数 (g 係数または g 値と呼ばれる)、β は電子磁気モーメントの自然単位 (ボーア磁子と呼ばれる) です。自由電子の g 値 = 2.00232、β = 9.2710 × 10-21 erg/Gauss、h = 6.62620 × 10-27 erg·s を上記の式に代入すると、電磁波周波数と共鳴磁場の関係は次のようになります: (ガウス) = 2.8025 (MHz)。
電子常磁性共鳴 (EPR) の試験装置の紹介
電子常磁性共鳴分光計は、1. マイクロ波発生および伝導システム、2. 共鳴空洞システム、3. 電磁石システム、4. 変調および検出システムの 4 つのコンポーネントで構成されています。
分光計の主な作業フローは次のとおりです。
1.RFパルス: 核磁気共鳴分光計は、サンプルにRFパルスを適用してサンプル内の核を励起します。このRFパルスの周波数は、通常、特定の核の共鳴周波数と一致します。
2.共鳴周波数の測定: 外部磁場の強度を徐々に増加させることにより、サンプル内の核は徐々に共鳴状態に達し、核の共鳴周波数を決定します。
3.検出信号: サンプル内の原子核が共鳴すると、信号が送信されます。この信号は検出器によってキャプチャされ、核磁気共鳴分光法に変換されます。
4.データ処理: キャプチャされた信号は、フーリエ変換などの数学的手法によって処理され、サンプル内のさまざまな核に関する情報を含む核磁気共鳴スペクトルに変換されます。
電子常磁性共鳴 (EPR) の研究対象
1. フリーラジカル: 分子にはジフェニルピクリルヒドラジル (DPPH)、トリフェニルメチルなどの不対電子物質が含まれており、不対電子を持っています。
2. ビラジカルまたはポリラジカル: 分子内に 2 つ以上の不対電子が含まれていますが、それらの不対電子は互いに離れており、相互作用は弱いです。
3. 三重項分子: この化合物の分子軌道には 2 つの不対電子が含まれており、それらは互いに非常に近く、互いに強い相互作用を持っています。酸素分子と同様に、基底状態または励起状態になることができます。
4. 遷移金属イオンと希土類イオン: これらの分子は、一般的な遷移金属イオン Ti3+ (3d1)、V3+ (3d7) など、原子軌道に不対電子として現れます。
5.固体の格子欠陥: 1 つ以上の電子または正孔が欠陥内またはその近くに閉じ込められ、面心、体心などの単一電子材料を形成します。
6. 水素、窒素、アルカリ金属原子などの奇数電子を持つ原子。
電子常磁性共鳴 (EPR) の応用
EPR 技術は、以下の分野で広く使用されています:
1. フリーラジカル中間体の直接検出と分析: フリーラジカルの EPR 検出は、高速で直接的かつ効果的な方法です。実験では、得られた EPR スペクトルの対応する吸収ピークの g 係数を計算します。標準値と比較することでフリーラジカルを推定し、次に化学的手段でフリーラジカルを除去して上記の推論を検証します。
2. EPR 検出法と一過性フリーラジカルの応用: フリーラジカル捕捉技術と EPR の組み合わせには、高い検出感度、強力な特異的選択性、信頼性の高い分析結果という利点があります。これは、寿命が短く定常濃度が低い一過性フリーラジカルの検出に広く使用されています。細胞や動物システム、化学反応メカニズムを含む多くの研究で広く使用されています。一過性フリーラジカルの EPR 検出の実験方法は次のとおりです: まず、フリーラジカルを捕捉できるプローブ分子を設計して合成します。このプローブ分子は、反応中に生成される一時的なフリーラジカルを迅速に捕捉できなければなりません。次に、捕捉反応付加物の分子構造をEPRで分析します。EPRライン上の各ピークの構造を1つずつ識別して、推測および識別します。
3.常磁性イオン錯体のEPRスペクトルの研究:常磁性イオン錯体のEPRスペクトルは、常磁性金属イオンを構造プローブとして使用し、タンパク質やその他の有機物質と結合して配位構造を形成します。常磁性イオン錯体のEPRスペクトルを研究することで、錯体の分子のスピン状態、配位構造、電子エネルギーレベルなどの重要な情報を得ることができます。常磁性イオンのEPRスペクトルの分析は、錯体の構成とd電子および欠陥の分布に依存します。理論計算方法の研究を通じて、さまざまな配位場におけるさまざまな遷移金属イオンとその化合物のEPR信号特性と触媒特性を詳細に分析できます。
4.固体の格子欠陥: 1 つ以上の電子または正孔が欠陥内または欠陥付近に閉じ込められ、面心、体心などの単一電子材料を形成します。または、原子の不足によって生じる単一電子を含む原子欠陥。
5.工業および農業生産における電子常磁性共鳴の応用: 電子常磁性共鳴は、食品およびフリーラジカル、ビール醸造プロセスの品質管理、放射線量計、考古学年代の決定、タバコのフリーラジカルの検出、種子および花粉の最適な保管条件の予測など、実際の工業および農業生産において多くの用途があります。
電子常磁性共鳴 (EPR) スペクトルの紹介と分析
パート 1: EPR スペクトルの紹介
1. EPR スペクトルの構成:
EPR スペクトルは横軸と縦軸で構成されます (図 3 を参照)。横軸には、磁場強度と g 係数の 2 つの表現があります。磁場強度の一般的な単位は mT と G で、それらの変換関係は 1 mT=10 G です。g 係数は無次元単位で、常磁性体の指紋とも呼ばれ、空孔/遷移金属イオンの価電子状態でよく使用されます。縦座標は信号強度 (強度) で、任意の単位で、一般的に a.u. が使用されます。
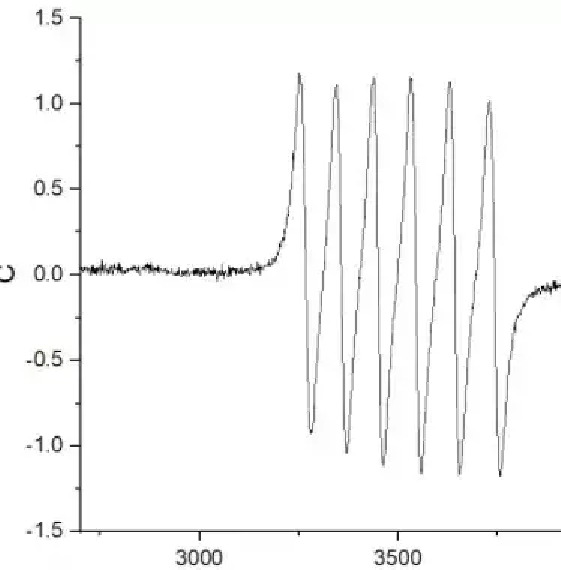
図 3 金属 Mn の EPR スペクトル
2. EPR スペクトルの線形、線幅、g 係数:
2.1 線形
図 4 に示すように、EPR の線形はローレンツ (上部) とガウス (下部) に分かれています。ローレンツ曲線の角は一定のラジアンを示し、ガウス曲線の角は同様の直角 90 ° を示します。
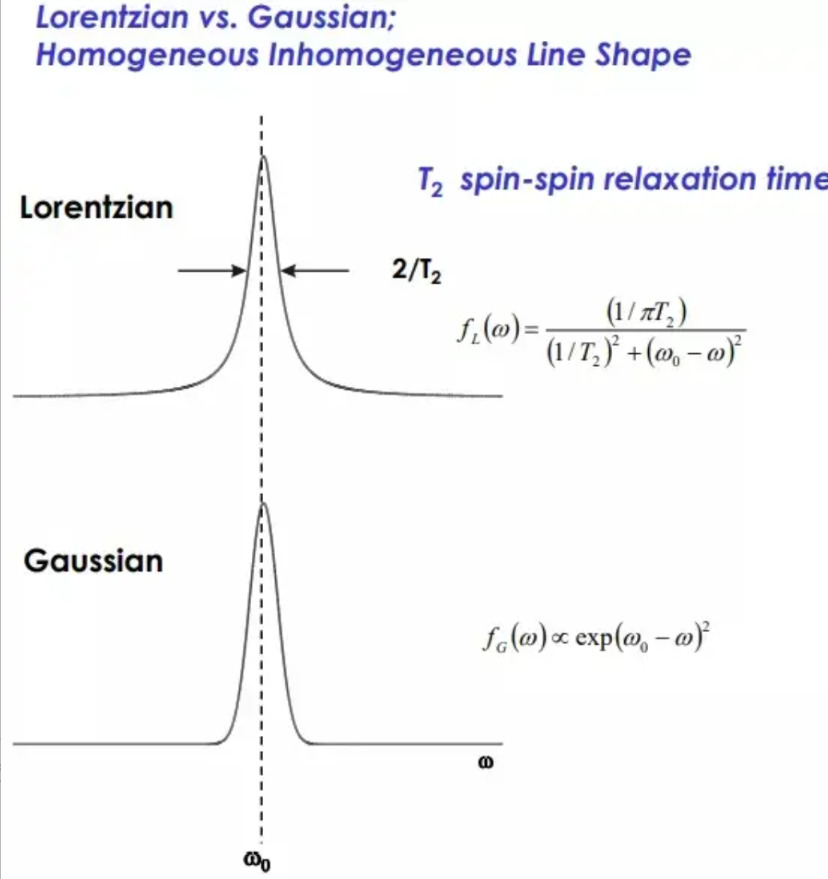
図 4 EPR スペクトルのローレンツ線とガウス線
2.2 線幅
図 5 に示すように、ピークの最高点と最低点の間の距離は ∆H または ∆B で示されます。この 2 つの間の距離がスペクトルの線幅であり、単位は通常ガウス (G) または mT です。
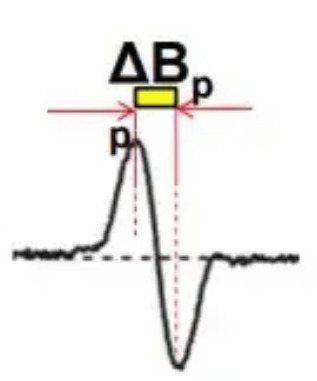
図 5 EPR スペクトルの線幅
2.3 g 係数
図 6 に示すように、単一ピークの g 係数はピークの中心に対応する磁場であり、二重ピークの g 係数は 2 つのピークの中心に対応する磁場であり、対称マルチピークの g 係数は中央ピークの中心に対応する磁場です。
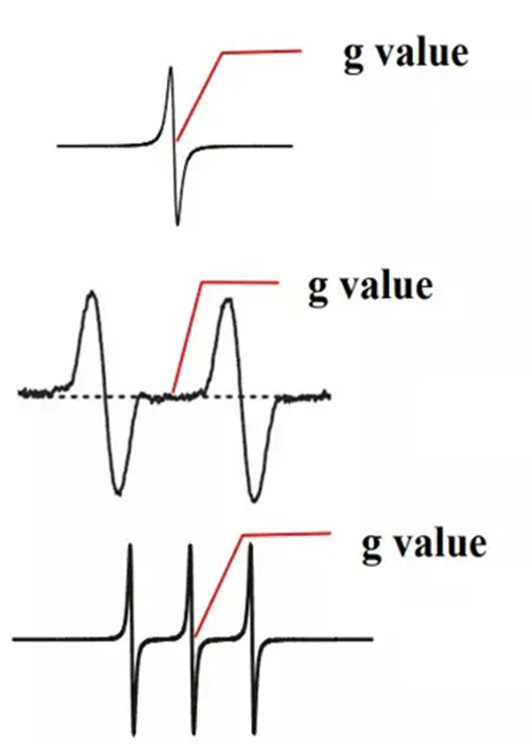
図 6 EPR スペクトルの g 係数の読み取り
パート 2: EPR スペクトルの簡単な分析
以下では、主に、ヒドロキシル ラジカル、スーパーオキシド ラジカル、一重項酸素、O、N、S 空孔のスペクトルなど、いくつかの一般的なフリーラジカルと空孔のスペクトル分析を紹介します。
フリーラジカルのスペクトルは主にピークの数と割合によって決まり、空孔は主に g 係数の値によって決まります。
1. ヒドロキシル ラジカル (OH)
図 7 に示すように、ヒドロキシル ラジカルは OH と呼ばれ、4 つのピークがあり、左から右にピークの比率は 1 : 2 : 2 : 1 です。
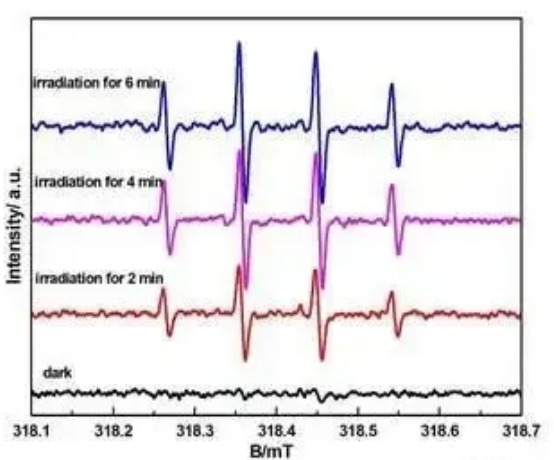
図 7 ヒドロキシルラジカルのスペクトル
2. スーパーオキシドラジカル (OO)
図 8 に示すように、スーパーオキシドラジカルは OO と呼ばれ、左から右に 4 つの大きなピークと 2 つの小さなピークの 6 つのピークがあります (1、2、4、6 の位置のピーク強度はほぼ同じで、3 と 5 の位置のピーク強度は低くなります)。
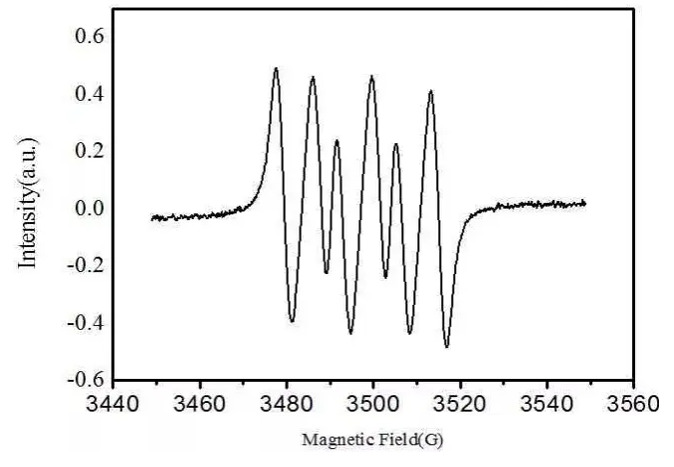
図 8 スーパーオキシドラジカルのスペクトル
3. 一重項酸素 (1O2)
図 9 に示すように、一重項酸素は 1O2 と呼ばれ、左から右に 3 つのピークがあり、高さは 1:1:1 です。
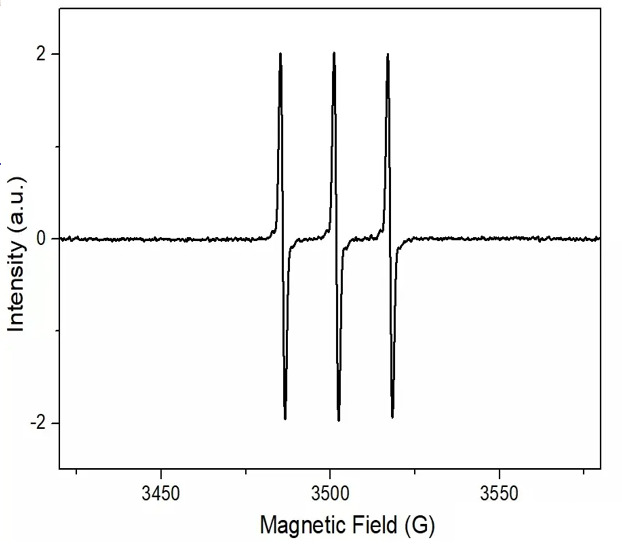
図 9 一重項酸素のスペクトル
4. 空孔
図 10 に示すように、空孔は主に g 因子の値に依存します。一般的な O 空孔は約 2.003、S 空孔は約 2.004、N 空孔は約 2.005 です。
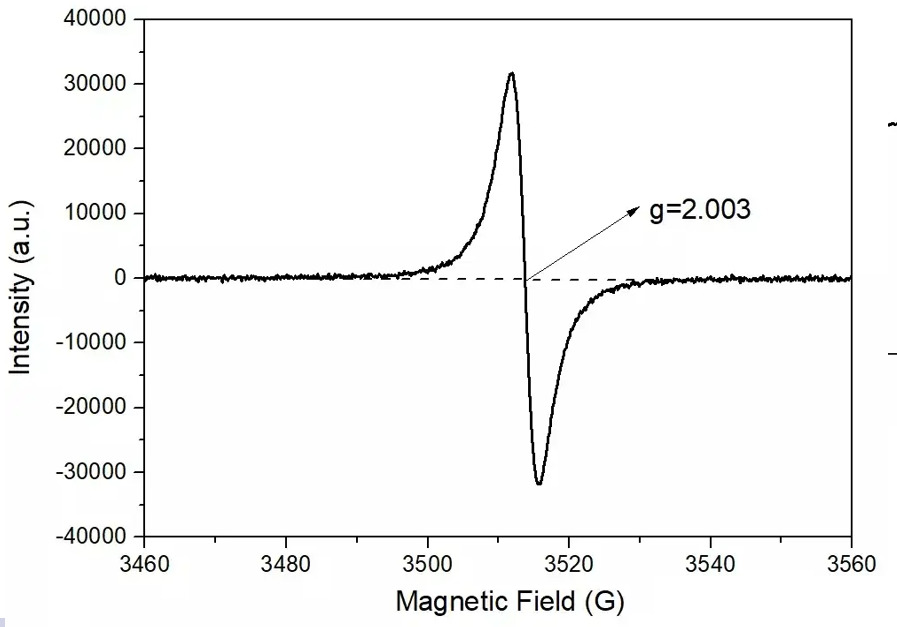
図10 空孔のスペクトル